

重庆将对接种问题百白破疫苗的儿童进行补种!教你如何鉴定问题疫苗
 沙坪坝微政务
沙坪坝微政务


昨晚23:35分,中国政府网发布消息:李克强总理就疫苗事件作出批示:此次疫苗事件突破人的道德底线,必须给全国人民一个明明白白的交代。
李克强在批示中要求,国务院要立刻派出调查组,对所有疫苗生产、销售等全流程全链条进行彻查,尽快查清事实真相,不论涉及到哪些企业、哪些人都坚决严惩不贷、绝不姑息。对一切危害人民生命安全的违法犯罪行为坚决重拳打击,对不法分子坚决依法严惩,对监管失职渎职行为坚决严厉问责。尽早还人民群众一个安全、放心、可信任的生活环境。
此前7月16日,李克强已就疫苗事件作出批示,要求彻查。
那么,重庆情况如何?
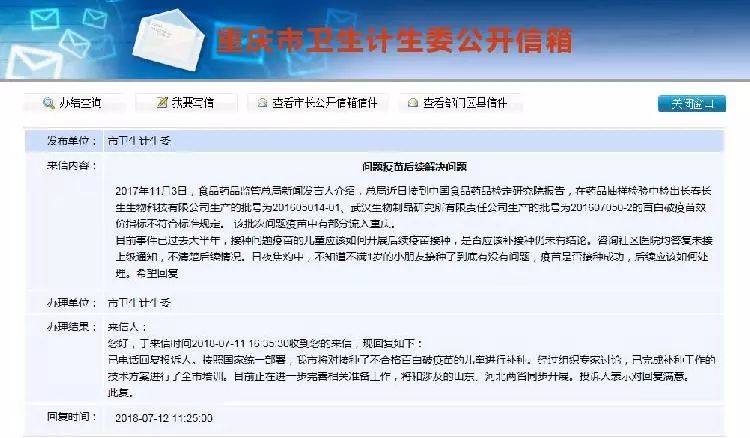
事实上,据重庆市卫生计生委官网消息,早在7月11日,就有市民向市卫计委公开信箱来信询问:
2017年11月3日,食品药品监管总局新闻发言人介绍,总局近日接到中国食品药品检定研究院报告,在药品抽样检验中检出长春长生生物科技有限公司生产的批号为201605014-01、武汉生物制品研究所有限责任公司生产的批号为201607050-2的百白破疫苗效价指标不符合标准规定。 该批次问题疫苗中有部分流入重庆。
目前事件已过去大半年,接种问题疫苗的儿童应该如何开展后续疫苗接种,是否应该补接种仍未有结论。咨询社区医院均答复未接上级通知,不清楚后续情况。日夜焦灼中,不知道不满1岁的小朋友接种了到底有没有问题,疫苗是否接种成功,后续应该如何处理,希望回复 。
重庆市卫生计生委7月12日回复如下:
已电话回复投诉人。按照国家统一部署,我市将对接种了不合格百白破疫苗的儿童进行补种。经过组织专家讨论,已完成补种工作的技术方案进行了全市培训。目前正在进一步完善相关准备工作,将和涉及的山东、河北两省同步开展。投诉人表示对回复满意。
另外,在7月18日,市疾控中心表示重庆已经全面停用长春长生生物科技有限责任公司生产的冻干人用狂犬病疫苗。如果已接种长春长生的狂犬病疫苗且尚未完成全程接种者,可使用另一品牌的人用狂犬病疫苗。
对于市民普遍关心的此次违法违规生产的冻干人用狂犬病疫苗有否流入重庆的问题?市疾控中心有关负责人说,按照国家药品监督管理局通报,此次飞行检查所有涉事批次产品,尚未出厂和上市销售,全部产品已得到有效控制。如果市民对前期接种的长春长生公司生产的冻干人用狂犬病疫苗存在疑问,建议咨询食品药品监督部门。
市疾控中心提醒,夏季是狂犬伤人事件的高发季节,如果被猫或犬咬伤或抓伤需及时接种狂犬病疫苗。目前我市人用狂犬病疫苗供应充足,具体接种地点请与当地疾控中心联系。
如何鉴定问题疫苗?
☟☟☟
同时,据记者最新消息,如果消费者在接种疫苗时,仍旧对疫苗的安全有所担心。即日起,消费者仅需打开手机淘宝、天猫、支付宝、阿里健康等App,扫描药盒上以数字8打头的20位追溯条形码,便可获得包含药品名称、厂家、批号、效期等相应信息。如果该盒疫苗已经被召回,扫码页上将在显著位置、以红色字体警示药品异常,并提示该药品已被召回,请勿使用。
7月22日,阿里健康“码上放心”在原有的药品“扫码验真”功能基础上,上线召回警示功能,针对此次疫苗造假事件中全部问题批次的狂犬疫苗进行连夜标定,并在手机移动端上打开多个App查询接口,使得消费者能够通过简单的手机扫码动作,即可自行排查问题疫苗。
此外,我们对大家关心的其他问题进行了梳理
一起来了解一下
问:事件相关的百白破疫苗到底都是哪些?
答:此次被爆出的百白破疫苗事件,实际上是去年年底的问题,具体包括两个生产企业,长春长生生物科技有限公司和武汉生物制品研究所有限责任公司。
问:事件相关的百白破疫苗到底出了什么问题?
答:百白破疫苗的主要问题是:效价指标不合格。
带来的后果是,可能影响免疫保护效果,但对人体没有危害。
国家药监局公告显示,百白破疫苗的主要问题,检验时发现 「效价测定」 项不符合规定。

问:打了「问题疫苗」后,会产生什么后果?是否可能有遗症?
答:这批疫苗,对人体的安全没有影响,最大的风险在于可能失效,导致无法预防对应的疾病。
很多家长担心孩子接种问题疫苗,会带来其他后遗症。
实际上,疫苗的常见不良反应包括局部的红肿热痛、发热、过敏等,一般都比较轻微。而过敏等比较严重的情况,发生率很低,对大多数人来说,疫苗是安全的。
疫苗产生的不良反应,多发生在接种后的 24~48 小时内,后期再发,或者产生后遗症的可能性很小。
问:如何确定是否接种了不合格的疫苗?万一接种到涉事的百白破疫苗怎么办?
答:家长可以查看儿童预防接种证上的百白破疫苗接种记录,对比疫苗生产企业和批号,也可以咨询当时的接种单位。
疫苗接种记录中,标注了疫苗批次和企业
▼
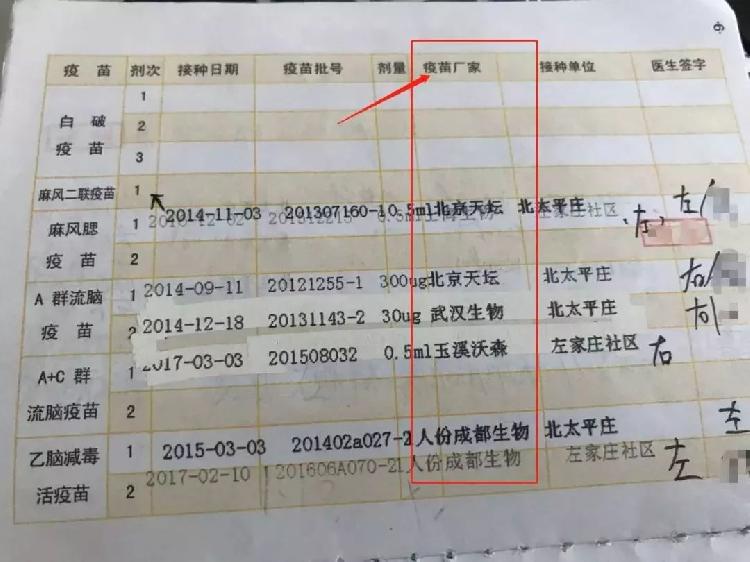
百白破疫苗需分别于 3、4、5 月龄和 18 月龄各接种 1 剂次,共接种 4 次。
正常来说,完成 4 次接种的儿童可得到较好的保护效果:
预防典型百日咳的效力约 85%;
破伤风的保护效力为 80~100%;
接种 3 次以上,对白喉的保护效力约为 95%。
而被爆出的两批次百白破疫苗,效价指标不合格,可能影响免疫保护效果。
家长如果确定孩子接种的是涉事的百白破疫苗,可以结合孩子接种的次数和批次情况,向当地疾控部门或接种单位咨询,看是否要继续补种。
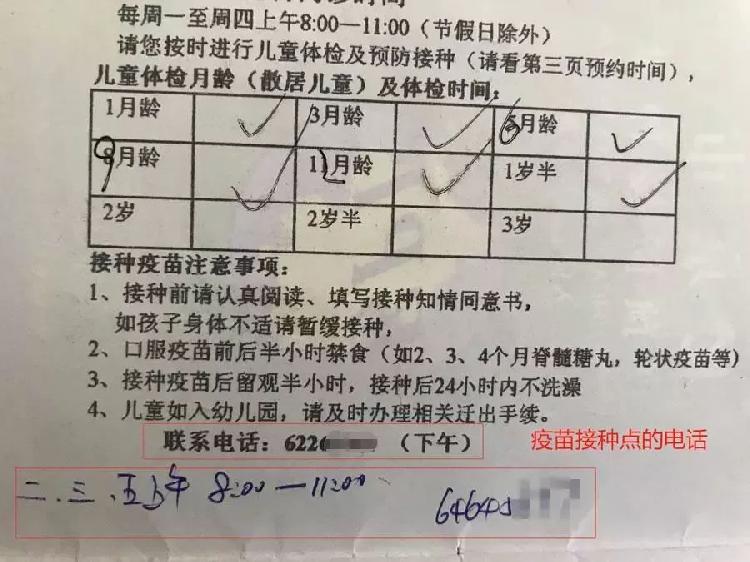
儿童预防接种证的第一页
标注了孩子户口所属接种单位的电话
▼
问:孩子还没接种百白破疫苗,能打吗?
答:能打。
百白破疫苗能有效预防三种危重疾病,目前出事的批次只有这两个批次,其他批次暂无问题。
而且,之前涉事的百白破疫苗已经停止接种,所以再去打的话并不会遇到,各位家长并不必太过担心。
千万不要因为担心疫苗有问题,就不给孩子注射。
如果家长实在有疑虑,可以优先接种联合疫苗,或者选择其他更加信赖的企业生产的疫苗。
问:我家孩子接种的其他类别的疫苗也是涉事企业的,是不是也需要补种?
答:暂时其他疫苗其他批次都没有出现问题,建议大家冷静,保持关注。
疫苗补种存在一定的风险,不要盲目补种。
问:为了防止接种到问题疫苗,我可以不给孩子打疫苗么?
答:不能因噎废食,因害怕而放弃疫苗接种,风险最高的还是孩子。
目前国家之所以能将白喉、百日咳和新生儿破伤风控制在较低水平,靠的就是极高接种率。
如果因为这些事件导致疫苗的恐慌,而拒绝一切接种的话,那受伤的必然是所有人。
国家药监局的监测数据显示,2008 年以来,国家药品抽检计划共抽检疫苗产品 944 批次,合格率 99.6%,也就是说,绝大部分疫苗非常安全。
一类疫苗所预防的乙肝、麻疹、百日咳,二类疫苗所预防的水痘,这些疾病对于孩子的健康都存在巨大的威胁。
所以,接种疫苗仍然是保护健康最好的手段,我们仍然应该坚持打疫苗。
疫苗是人类对抗传染性疾病最有利的武器,足够多的人接种疫苗,才能够形成广泛的、有力的防御。
本文由“壹伴编辑器”提供技术支持
长春长生违规疫苗事件梳理
7月15日,国家药品监督管理局发布通告:国家药监局根据线索组织检查组对长春长生生物科技有限责任公司(以下简称“长春长生”)生产现场进行飞行检查。检查组发现,长春长生在冻干人用狂犬病疫苗生产过程中存在记录造假等严重违反《药品生产质量管理规范》(药品GMP)行为。根据检查结果,国家药监局迅速责成吉林省食品药品监督管理局收回长春长生相关《药品GMP证书》。通告称,所有涉事批次产品尚未出厂和上市销售。

7月16日,长生生物发布公告,表示正对有效期内所有批次的冻干人用狂犬病疫苗全部实施召回。
7月17日,长春长生发声明称,此次所有涉事疫苗尚未出厂销售,所有已经上市的人用狂犬病疫苗产品质量符合国家注册标准。然而,长春长生单方面的质量保证并不能给公众信心,尤其是近几年使用过其疫苗的人们,担忧情绪日渐积累。
7月18日,山东疾控中心发布信息,宣布山东省已全面停用长春长生生物科技有限责任公司生产的人用狂犬病疫苗。
此时,事件的发展似乎仍在可控范围。但仅仅两天后,舆论彻底失控。
7月20日,吉林省食药监局的一纸行政处罚公示,彻底将公众的早已郁积多日的愤怒情绪引爆:长春长生生产的“吸附无细胞白百破联合疫苗”(批号:201605014-01)经中国食品药品检定研究院检验,检验结果[效价测定]项不符合规定,按劣药论处。这条处罚信息,针对的是2017年11月的一起违法事件。由长春长生生物科技有限公司和武汉生物制品研究所有限责任公司生产的各一批次共计65万余支百白破疫苗效价指标不符合标准规定,食药监总局已责令企业查明流向,并要求立即停止使用不合格产品。

2016年,长春长生公司1批(21.0048 万人份)百白破疫苗因“无细胞百日咳疫苗效价测定”被拒签。 中检院《2016年生物制品批签发年报》 资料图
经查,长春长生生物科技有限公司生产的批号为201605014-01的疫苗共计252600支,全部销往山东省疾病预防控制中心;武汉生物制品研究所有限责任公司生产的批号为201607050-2的疫苗共计400520支,销往重庆市疾病预防控制中心190520支,销往河北省疾病预防控制中心210000支。
长生生物回应称:
百白破生产车间已停产将制定纠正措施
长生生物7月22日晚间回复深交所称,目前,公司百白破生产车间已经停产,公司正积极研究百白破组份疫苗以及以此为基础的多联疫苗。对于此次事件的发生,我们感到十分的自责和愧疚,再次向各位接种者和投 资者表示深深的歉意。公司将引以为戒,举一反三,制定切实可行的纠正措施,进行彻底整改,确保生产的合规性、真实性、可靠性、可追溯性以及疫苗质量的安全性。
长生生物收到证监会调查通知书,
或存退市等风险,下午复牌
7月23日,长生生物科技股份有限公司发布公告称长生生物科技股份有限公司收到中国证券监督管理委员会《调查通知书》(苏证调查通字 2018074 号),公司因涉嫌信息披露违法违规被立案调查。如果公司因前述立案调查事项被监管部门最终认定存在重大违法行为或移送公安机关,根据《深圳证券交易所股票上市规则》的有关规定,公司股票可能存在被实施退市风险警示、暂停上市或终止上市的风险。
为维护广大投资者利益,保证公平信息披露,避免造成公司股价异常波动,根据《深圳证券交易所股票上市规则》的相关规定,经向深圳证券交易所申请,公司股票(证券简称:002680,证券代码:长生生物)自 2018 年 7 月 23 日开市起停牌。
于 2018 年 7 月 23 日下午开市起复牌。
但网友对这个回应并不满意
他们认为
↓
这轮得到你自己停产?

还想整改?这分明是犯罪!

国家药监局通报长生疫苗案件情况
“已对企业立案调查”
国家药监局负责人昨天通报长春长生生物科技有限责任公司违法违规生产冻干人用狂犬病疫苗案件有关情况。
根据举报提供的线索,7月5日,国家药监局会同吉林省局对长春长生公司进行飞行检查;7月15日,国家药监局会同吉林省局组成调查组进驻企业全面开展调查。7月15日,国家药监局发布了《关于长春长生生物科技有限责任公司违法违规生产冻干人用狂犬病疫苗的通告》。
现已查明,企业编造生产记录和产品检验记录,随意变更工艺参数和设备。上述行为严重违反了《中华人民共和国药品管理法》《药品生产质量管理规范》有关规定,国家药监局已责令企业停止生产,收回药品GMP证书,召回尚未使用的狂犬病疫苗。国家药监局会同吉林省局已对企业立案调查,涉嫌犯罪的移送公安机关追究刑事责任。
按照疫苗管理有关规定,所有企业上市销售的疫苗,均需报请中国食品药品检定研究院批签发,批签发过程中要对所有批次疫苗安全性进行检验,对一定比例批次疫苗有效性进行检验。该企业已上市销售使用疫苗均经过法定检验,未发现质量问题。为进一步确认已上市疫苗的有效性,已启动对企业留样产品抽样进行实验室评估。
另据中国疾病预防控制中心监测,我国的狂犬病发病率近年来逐步下降。
药监局已部署全国疫苗生产企业进行自查,确保企业按批准的工艺组织生产,严格遵守GMP生产规范,所有生产检验过程数据要真实、完整、可靠,可以追溯。国家药监局将组织对所有疫苗生产企业进行飞行检查,对违反法律法规规定的行为要严肃查处。
负责人说,该企业是一年内被第二次发现产品生产质量问题。去年10月,原食药监总局抽样检验中发现该企业生产的1批次百白破疫苗效价不合格,该产品目前仍在停产中,有关补种工作原国家卫计委会同原食药监总局已于今年2月进行了部署。
总结:现已查明
企业编造生产记录和产品检验记录,
随意变更工艺参数和设备。
上述行为严重违反了《中华人民共和国药品管理法》《药品生产质量管理规范》有关规定,国家药监局
已责令企业停止生产,
收回药品GMP证书,
召回尚未使用的狂犬病疫苗。
国家药监局会同吉林省局
已对企业立案调查,
涉嫌犯罪的移送公安机关追究刑事责任。
新华社等纷纷发文要求,对于问题疫苗,一定要一查到底,依法严惩!
这次事件对食药监管理再次敲响警钟,
相关部门须一查到底!

主办单位: 沙坪坝区委宣传部、区委网信办
主编:蒋频 编辑:金永元
(沙坪坝微政务整理于重庆日报)

传播权威声音、传递主流价值、凝聚思想共识、汇聚全民力量。



