美国食品药品管理局批准瑞德西韦用于治疗新冠住院患者。
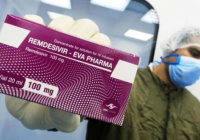
澎湃新闻消息,当地时间10月22日,美国食品药品管理局(FDA)批准了吉利德科学的抗病毒药物瑞德西韦用于治疗新冠住院患者,成为美国首个正式获批的新冠治疗药物。
瑞德西韦将以Veklury商品名出售,可用于美国成人和儿童新冠住院患者(12岁及以上,体重至少40公斤)。FDA强调,瑞德西韦仅能在提供与住院医院护理相当的急性护理的医院或护理机构中使用,对瑞德西韦或其任何成分过敏的患者禁用该药。
受上述利好消息,吉利德盘后股价涨逾5%。
此次批准基于三项随机对照试验,包括近期发表的三期临床试验结果。吉利德科学在10月8日公布了瑞德西韦三期临床数据,这些数据来自美国国家过敏和传染病研究所(NIAID)领导的生物随机双盲安慰剂对照的3期研究,涵盖了全球约1060例住院患者。数据显示,接受瑞德西韦治疗的住院患者平均恢复时间快了五天,而患有严重疾病的患者则快了七天,而这些重病患者占研究总数的85%。
今年5月1日,FDA曾为瑞德西韦发放了治疗新冠肺炎的紧急使用授权(EUA),根据该授权,瑞德西韦可用于治疗疑似或实验室确诊的成人和儿童新冠肺炎重症住院患者。
需要注意的是,对于瑞德西韦此次正式获批,FDA表示,不包括最初于2020年5月1日发布的根据紧急使用授权(EUA)被授权使用瑞德西韦的全部人群。评估瑞德西韦在儿科患者人群中的安全性和有效性的临床试验正在进行中。
FDA表示,为了确保先前受EUA覆盖的儿童人群,FDA修订了瑞德西韦的紧急使用权。根据授权,瑞德西韦可用于疑似或实验室确诊的新冠住院儿童患者的治疗,具体包括用于体重3.5公斤至40公斤以下的住院儿童患者或12岁以下体重至少3.5公斤的住院儿童患者。
值得注意的是,世卫组织此前曾表示,瑞德西韦等对改善新冠肺炎住院患者病亡率影响不大。吉利德对此回应称,该试验数据未经严格的审查。
在三期临床试验公布之前,瑞德西韦已经凭借前期研究数据在50多个国家/地区获得治疗新冠肺炎不同程度的批准或授权。
在8月6日吉利德科学在一份声明中提到,瑞德西韦的制造网络现已包括北美、欧洲和亚洲的40多家公司。自1月以来,瑞德西韦的供应量已增长了50倍以上,并有望从10月开始满足全球实时需求。
原标题:瑞德西韦获FDA正式授权,成为全美首个获批新冠治疗药物
【免责声明】上游新闻客户端未标有“来源:上游新闻-重庆晨报”或“上游新闻LOGO、水印的文字、图片、音频视频等稿件均为转载稿。如转载稿涉及版权等问题,请与上游新闻联系。