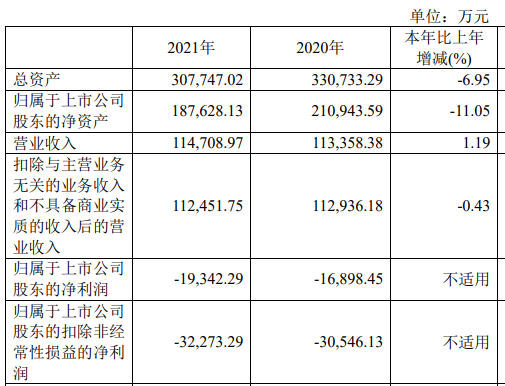
人民日报健康客户端 消息,人民日报健康客户端根据国家药监局、各药企公告梳理发现,我国国产小分子新冠口服药已有10余款在紧急研发中,多款国产新冠口服药已进入三期临床试验。
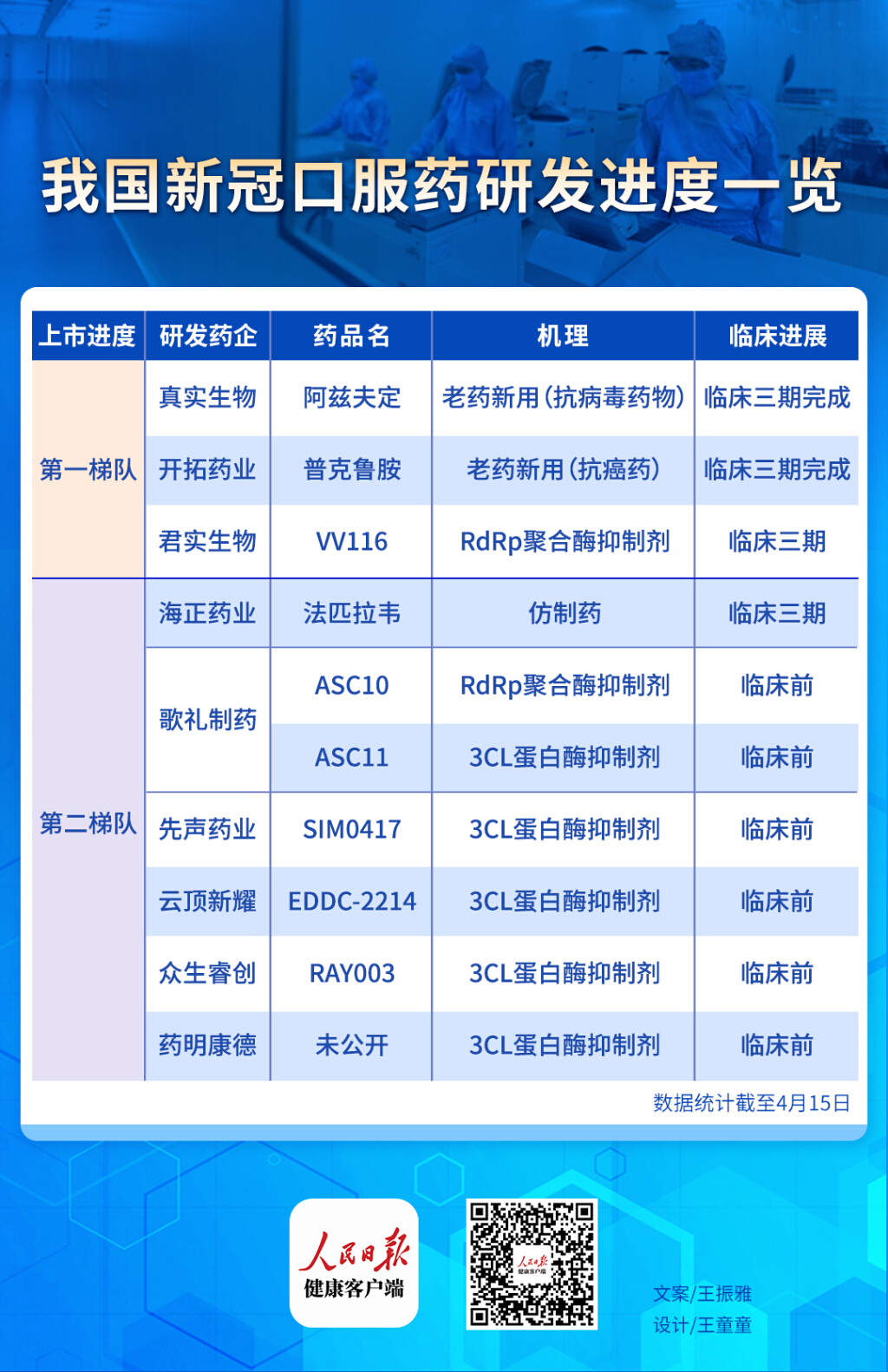
人民日报健康客户端记者采访多位新冠口服药研发人员均表示,新冠口服药研发方面不存在技术难题,建议在临床试验、审批方面通道畅通,今年内都有可能上市。
第一类新冠口服药为“老药新用”技术路线,即通过对原有以上市的抗病毒药、抗肿瘤药物,进行临床试验,在剂量、剂型进行研究,研发出新冠病毒的新适应症。例如阿兹夫定、普克鲁胺。“老药新用”路线的优点就是,药物本身作用机理清楚,临床试验研发快,两款药物均已处于三期临床完成阶段。阿兹夫定、普克鲁胺与国外两款新冠药物属同一时期进入临床三期。
第二类新冠口服药为以RdRp聚合酶抑制剂和3CL蛋白酶抑制剂的小分子新药研发。而这两类药物由于临床试验阶段较晚,目前有VV116与法匹拉韦进入临床三期。
第三类药物为已上市的两款新冠口服药的仿制药。多位新冠口服药研发人员向人民日报健康客户端表示,遇到的瓶颈在临床试验。
歌礼制药创始人吴劲梓介绍,国家药监局新冠药临床研究指南建议进行安慰剂对照临床试验,但病人在医院归各地卫生系统管理,各地卫生系统因为抗疫的需要,不允许用病人做安慰剂对照试验,尤其是重症病人。因为,安慰剂对照试验就意味着,一部分重症病人服用药物,一部分重症病人使用无药效的安慰剂进行临床观察。
有的专家建议,要明确国产抗新冠药物在大疫发生时的紧迫性,把握主要关键技术指标,减少审批环节,对于新冠口服药开通并真正落实“优先审批”,加速药物审评速度。
关于新冠口服药临床试验难做的问题。君实生物首席执行官李宁认为,加强机制体制创新,专班应优化国内病人资源,联合各地卫生健康部门,合理调配临床试验病人,保证临床试验的正常有序进行。此外,也应该开展紧急使用授权通道机制,让数据效果好的药物进入紧急使用,附条件上市,后续再完善临床数据。
原标题:多款国产新冠口服药进入三期临床,专家建议加速审评
【免责声明】上游新闻客户端未标有“来源:上游新闻”或“上游新闻LOGO、水印的文字、图片、音频视”等稿件均为转载稿。如转载稿涉及版权等问题,请联系上游。