澎湃新闻消息,3月20日,国家食品药品监督管理总局就此前遭质疑的儿科药物“匹多莫德”连发两份通知,分别要求瑞士普利化学工业公司尽快启动临床有效性试验、要求六地食药监局督促行政区域内匹多莫德制剂生产企业尽快启动临床有效性试验。
上述评价结果均要求在3年内报国家食品药品监督管理总局药品审评中心。
在上述国家食药监总局发布的两份通知中,总局均表示“鉴于医务界部分医生对匹多莫德制剂疗效提出质疑,食品药品监管总局药品审评中心组织专家进行了论证。”
澎湃新闻今年1月8日报道,拥有百万粉丝的“微博大V”、中国协和医科大学药学硕士冀连梅在一篇文章中指出,匹多莫德被广泛用于儿科、耳鼻喉科和皮肤科,每年销售额数十亿,但检索国内外权威文献库,却发现几乎未有太多值得信服的大样本临床试验数据证实此药的有效性和安全性。
今年3月9日,国家食品药品监督管理总局网站还发布了《关于修订匹多莫德制剂说明书的公告》,决定对匹多莫德制剂(包括匹多莫德片、匹多莫德散、匹多莫德分散片、匹多莫德口服溶液、匹多莫德口服液、匹多莫德胶囊、匹多莫德颗粒)说明书进行修订。总局发布的《匹多莫德制剂说明书模板》将该药品的适应症限定为:用于慢性或反复发作的呼吸道感染和尿路感染的辅助治疗。
【附】
总局关于匹多莫德口服液启动临床有效性试验的通知
食药监药化管函〔2018〕31号
2018年03月20日 发布
瑞士普利化学工业公司北京代表处:
鉴于医务界部分医生对匹多莫德制剂疗效提出质疑,食品药品监管总局药品审评中心组织专家进行了论证。经研究,请你单位通知匹多莫德口服液(注册证号:H20150635)公司POLICHEM S.R.L按照《中华人民共和国药品管理法》的有关规定,尽快启动临床有效性试验,并于3年内将评价结果报国家食品药品监督管理总局药品审评中心。
食品药品监管总局
2018年3月16日
总局关于匹多莫德制剂有关事宜的通知
食药监药化管函〔2018〕32号
2018年03月20日 发布
北京、天津、河北、内蒙古、江苏、浙江省(区、市)食品药品监督管理局:
鉴于医务界部分医生对匹多莫德制剂疗效提出质疑,食品药品监管总局药品审评中心组织专家进行了论证。经研究,请你局按照《中华人民共和国药品管理法》的有关规定,督促行政区域内匹多莫德制剂生产企业尽快启动临床有效性试验,并于3年内将评价结果报国家食品药品监督管理总局药品审评中心。
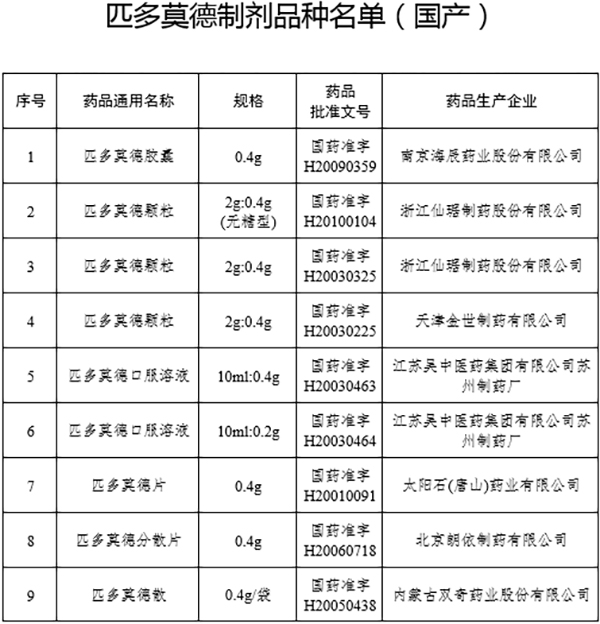
附件:匹多莫德制剂品种名单(国产)
食品药品监管总局
2018年3月16日
原标题:食药监总局发函:督促匹多莫德企业尽快启动临床有效性试验
【免责声明】上游新闻客户端未标有“来源:上游新闻-重庆晨报”或“上游新闻LOGO、水印的文字、图片、音频视频等稿件均为转载稿。如转载稿涉及版权等问题,请与上游新闻联系。